

─ 他の感染症や疾病マーカーへの適用拡大にも期待 ─
新型コロナウイルスなどの感染症において、これまで診断とウイルス量の同定にはPCR(注3)やELISA(注4)などの手法が用いられてきました。しかしながらどちらも時間がかかる上、検体量を多く必要とし、操作が複雑で検査者がウイルスに暴露される可能性があるなど、多くの課題がありました。
東北大学材料科学高等研究所(WPI-AIMR)の藪浩教授(主任研究者、同研究所水素科学GXオープンイノベーションセンター副センター長)、同大災害科学国際研究所の児玉栄一教授、同大マイクロシステム融合研究開発センターの戸津健太郎教授、および医療・ヘルスケア用診断機器開発などを手掛ける株式会社ハプロファーマ(仙台市、大滝義博社長)からなる研究グループは、マイクロ流路チップと蛍光測定による新しい定量検査システム「Express Biochecker」を開発しました。片面に蛍光発光色素、反対面に磁性粒子と抗体を結合したサブミクロンサイズのヤヌス粒子をプローブとして用いることが特徴です(図1)。本システムを用いると、わずか数十µLの検体から新型コロナウイルス(SARS-CoV-2)のNタンパク量(注5)を15分で定量測定することが可能になります。SARS-CoV-2の検査だけでなく、様々な感染症や疾病マーカー(生物指標化合物)を高感度に定量する新たなシステムとして期待される成果です。
本研究成果は現地時間8月15日に米国化学会(American Chemical Society)におけるコロイド・界面科学分野の代表的な専門誌であるLangmuirのオンライン速報版に掲載され、Supplementary Coverとしても採用されました。
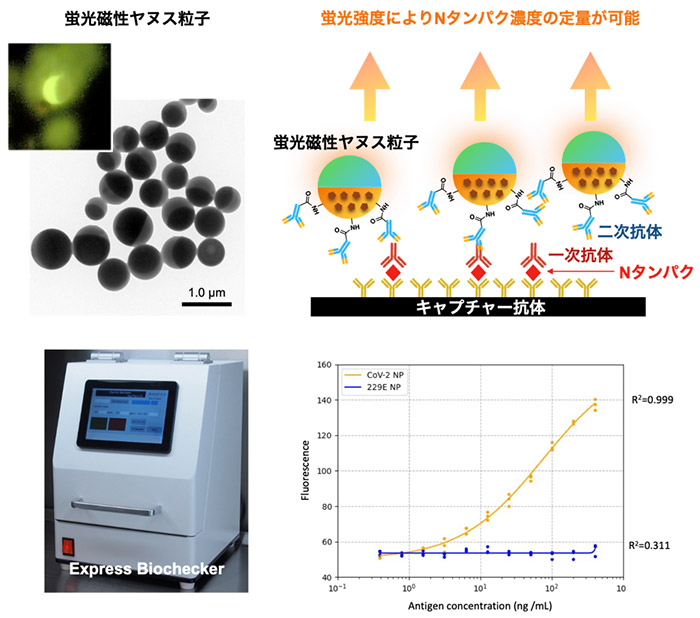
図1. 蛍光磁性ヤヌス粒子の透過型電子顕微鏡像と蛍光像(左上)と抗体結合蛍光磁性ヤヌス粒子を用いたNタンパク質検出の模式図(右上)、本研究で開発したExpress Biocheckerの外観図(左下)、および新型コロナウイルス(CoV-2, 黄色)とコロナウイルス(229E, 青色)のNタンパクの濃度測定結果(右下)。
近年新型コロナウイルスなどの感染症検査に対する要求の高まりから、高感度で定量的な抗原検査技術の開発が求められています。新型コロナウイルス(SARS-CoV-2)の感染は依然として世界的な公衆衛生の脅威となっており、PCRはその確定診断に広く使用されていますが、核酸増幅に時間がかかるため、診断が遅れるという欠点があります。一方、免疫クロマトグラフィーは、SARS-CoV-2感染を迅速に診断するために有用ですが、測定感度が低いため、偽陰性率が高くなる可能性があります。これらの理由から、簡便で迅速、かつ低コストな定量的免疫測定システムの開発は、臨床現場での迅速な診断において非常に重要です。
抗原検査には、ELISAはその高い精度と多様なターゲットタンパク質に対する適用性から広く使用されています。基材に固定した抗体と、呈色(ていしょく:発色または変色)や蛍光発光するプローブを結合した抗体で抗原を挟み込み、抗原を認識するサンドイッチアッセイが通常用いられています。高感度で定量的な検査のためには、抗原を高感度に認識する抗体セットだけでなく、少ない検体量で、高感度な定量測定が可能なプローブが必要です。
これまで研究グループでは、高分子を有機溶媒に溶かした溶液に高分子の貧溶媒(注6)を加え、良溶媒(注6)を蒸発除去することにより、高分子微粒子を得る「自己組織化析出(Self-ORganized Precipitation、SORP)法を独自に開発し、ポリスチレン(PS)とアミノ末端ポリブタジエン(PB-NH2)、および蛍光色素と有機分子で被覆した酸化鉄ナノ粒子を混合した溶液から各半球が異なる高分子からなるヤヌス型の微粒子が得られることを見出しました(参考文献1)。また、アミノ末端ポリブタジエンに抗体が結合できること(参考文献2)、磁場によって蛍光磁性ヤヌス粒子を配向させることで、蛍光強度を増強することができることを見出しています(参考文献3)。そこで、蛍光色素を導入した半球と逆側に抗体を結合することで、高感度な抗原抗体反応を検出するプローブとして活用できるのではないかと考えました。
こで研究グループは、国立研究開発法人日本医療研究開発機構(AMED)の支援を受け、蛍光磁性ヤヌス粒子を用いた検査システムの開発に2016年に着手。2020年からはSARS-CoV-2ウイルスのNタンパクをターゲットとし、その定量測定システムの開発を行いました。
SARS-CoV-2などの感染症診断には、
などの条件をクリアする必要があります。そこで、廃液の封じ込めが可能なマイクロ流路チップ中で抗原抗体反応を行い、蛍光磁性ヤヌス粒子の蛍光強度で高感度にNタンパクを計測するシステムを構築しました。
二次抗体をクロスカップリングによりサブミクロンサイズの蛍光磁性ヤヌス粒子の磁性粒子側に固定化し、抗体結合蛍光磁性ヤヌス粒子を作製しました(図2)。これにより、抗体が結合した反対面の蛍光部位が抗原抗体反応後に必ず上面を向く仕組みが成立します。
マイクロ流路チップは流路と検査部位、および廃液トラップから構成され、検査部位にキャプチャー抗体を固定してあります(図3)。検体や一次抗体、および抗体結合蛍光磁性ヤヌス粒子は開発した装置「Express Biochecker」中で自動的にピペッティングされ、流路チップに導入され、検査後チップごと廃棄することで検査者の感染を完全に防ぐことが可能です。また、数十µLと非常に少ない検体量で測定が可能です。
抗体セットを最適化することで、SARS-CoV-2のNタンパクと、従来型のコロナウイルスNタンパク(E226)の定量測定結果(図4)から、高い選択性と3.1 ng/mLの感度が実現できることが明らかとなりました。従来の研究から、感染者は数ng/mL以上のNタンパク量であることから、新型コロナウイルスの定量診断に有効であると考えられます。
今回はSARS-CoV-2を対象としましたが、本システムは抗体セットを変えることで様々な感染症や疾病マーカーに適用できる可能性があります。研究チームは今後、インフルエンザやウイルス性肝炎などでの適用も検討する予定です。
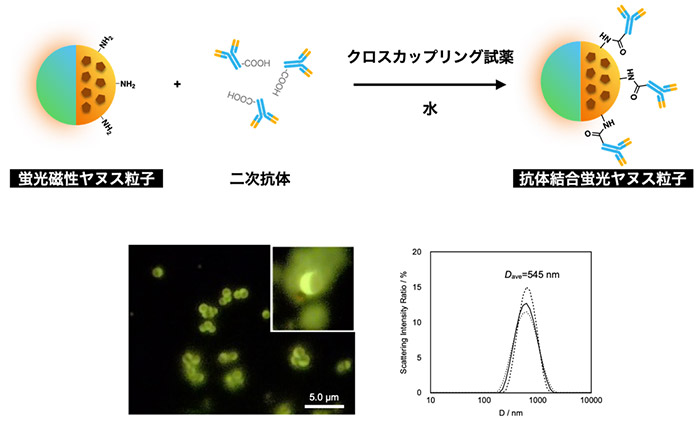
図2.抗体結合蛍光磁性ヤヌス粒子の作製方法(上)と、蛍光像(左下)および粒径分布(右下、N=3)。
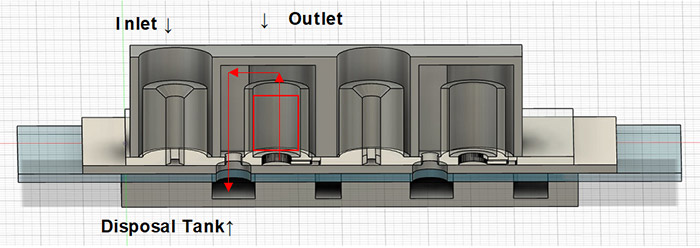
図3.マイクロ流路チップの構成
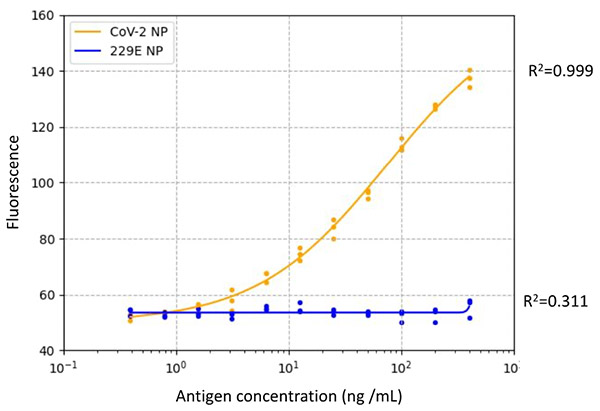
図4.SARS-CoV-2、E226 Nタンパクの定量測定結果
本研究の一部はAMED先端計測分析技術・機器開発プログラム、AMEDウイルス等感染症対策に資する医療機器・システム等の実証・改良研究支援、AMED令和2年度「新興・再興感染症に対する革新的医薬品等開発推進研究事業(新型コロナウイルス感染症(COVID-19)に対する研究)」に係る公募(5次公募)および科学研究費(JP19KK0357, JP20K20341, JP20H04625)の支援を受けて行われました。
| タイトル: | Janus-Type Immunofluorescent Probes and a Quantitative Immunoassay System |
|---|---|
| 著者: | H. Yabu, M. Suzuki, K. Matsukawa, I. Maeda, S. Ihara, K. Yaegashi, K. Totsu, H. Hayashi, E. Kodama |
| 掲載誌: | Langmuir |
| DOI: | 10.1021/acs.langmuir.4c01911 |
東北大学材料科学高等研究所(WPI-AIMR)
教授 藪 浩(やぶ ひろし)(研究者プロフィール)
| Tel: | 022-217-5996 |
|---|---|
| E-mail: | hiroshi.yabu.d5@tohoku.ac.jp |
東北大学材料科学高等研究所(WPI-AIMR) 広報戦略室
| Tel: | 022-217-6146 |
|---|---|
| E-mail: | aimr-outreach@grp.tohoku.ac.jp |
株式会社ハプロファーマ
中央研究所・解析センター
| Tel: | 022-272-2275 |
|---|