

-ペロブスカイト型水素化物の形成過程を解明-
東北大学金属材料研究所(所長 新家光雄。以下「東北大金研」という。)の研究グループは、同学原子分子材料科学高等研究機構(機構長 小谷元子。以下「東北大AIMR」という。)、独立行政法人日本原子力研究開発機構(理事長 鈴木篤之。以下「原子力機構」という。)との共同研究により、ペロブスカイト型水素化物の形成機構を大型放射光施設SPring-8の高輝度放射光X線を用いて世界で初めて解明しました。機能性材料として期待される一方、その合成報告例が限られていたペロブスカイト型水素化物の設計・開発指針が得られたことにより、水素貯蔵や超伝導などの機能性に富んだエネルギー材料開発が大いに加速されることになります。
ペロブスカイト構造(注1)は酸化物で良く知られており、これまでに超伝導、強誘電性、イオン伝導など多様な物性・機能性を示すペロブスカイト型酸化物が合成されており、圧電素子などの実用材料として利用されています。酸素原子を水素原子で置き換えたペロブスカイト型水素化物(注2)は水素貯蔵特性に加えて、酸化物と同様に多様な物性・機能性を示すものと期待されていますが、これまで合成に成功した水素化物は限られています。ペロブスカイト型水素化物はメカノケミカル法(注3)で合成されてきましたが、その形成過程の観察は困難であり、未解明であることから新たなペロブスカイト型水素化物の開発が停滞していました。
研究グループでは、第一原理計算(注4)による理論予測に基づいて新しいペロブスカイト型水素化物LiNiH3の合成に成功しました。その合成には、水素化リチウム(LiH)とニッケル(Ni)金属の混合粉体を高温高圧水素流体によって水素化する手法を用い、結晶性の良いペロブスカイト型水素化物を焼結体として合成することができます。高温高圧下の水素化反応過程を高輝度放射光X線を使った時分割X線回折法(注5)によって観測することにより、ペロブスカイト型水素化物LiNiH3の形成過程を明らかにしました。それによると、LiHとNi金属が水素化反応によって直接ペロブスカイト型水素化物が形成されるのではなく、3段階の反応、ステップ(Ⅰ):ニッケル水素化物(NiH)の形成、ステップ(Ⅱ):LiHとNiHの固溶体LiyNi1-yHの形成(注6)、ステップ(Ⅲ):固溶体の水素吸収によるペロブスカイト型水素化物LiNiH3の形成、によって段階的に形成されること、ステップ(Ⅱ)の固溶体水素化物LiyNi1-yHの形成がペロブスカイト形成の前駆状態であることが明らかにされました。
解明された形成過程から、固溶体水素化物を形成しうる元素の組み合わせを選ぶことがペロブスカイト型水素化物の合成に繋がるとの設計・開発指針が得られ、新しいペロブスカイト型水素化物の合成研究に向けての突破口が開かれたことになります。それに伴い、水素貯蔵や超伝導などの物性・機能性発現研究が本格化するものと期待されます。 この研究成果は、東北大金研 佐藤龍太郎 博士研究員、高木成幸 助教、松尾元彰 講師、青木勝敏 上級研究員、東北大AIMR折茂慎一 主任研究者(兼任 東北大金研 教授)、原子力機構 齋藤寛之 副主任研究員、遠藤成輝 博士研究員との共同研究によるもので、その一部は内閣府最先端・次世代研究開発支援プログラム「水素化物に隠された物性と機能性 —水素の存在状態の根源的探求からエネルギーデバイス実証へ」の支援を受け、SPring-8の利用研究課題として実施されました。
本研究成果は、3月4日に米国科学雑誌『Applied Physics Letters』のオンライン版に掲載されました。
ペロブスカイト型酸化物(化学式ABX3)は結晶構造がシンプルながら、多様な電気的・磁気的性質を示すことから、物性・機能性の宝庫と呼ばれており、これまで数多くのペロブスカイト型酸化物(化学式ABO3)が合成されています。圧力を加えると、圧力に比例した分極が生じる、すなわち圧電性を示すチタン酸バリウムや低温で電気抵抗がゼロになる、すなわち超伝導特性を示す酸化物高温超電導体などが代表的な物質例で、これらはペロブスカイト型構造あるいはペロブスカイト型構造を基礎とする結晶構造をとることが知られています。
酸素原子イオン(O2-)の一部あるいは全部を水素原子イオン(H-)に置き換えることによる、物性・機能性に富んだペロブスカイト型水素化物の合成の試みが最近始まりました。チタン酸バリウムでは酸素原子の一部を水素原子で置換することにより、電気を通さなかった絶縁体が導電性物質に変わることが見出されています。また、多くのペロブスカイト型酸化物が絶縁体であるのに対して、最近合成されたペロブスカイト型水素化物CaNiH3は金属であるとの理論予測がなされています。このようにペロブスカイト型水素化物はそれ自体が持つ水素貯蔵材料としての機能に加えて、酸化物とは異なるが、酸化物と同様に多様な物性・機能性を示すものと期待されています。
本研究の目的は新規ペロブスカイト型水素化物の合成手法を開発することにあります。そのために第一原理計算による安定なペロブスカイト型水素化物の探索と高輝度放射光X線回折測定によるペロブスカイト型水素化物の形成機構の解明実験を実施しました。ペロブスカイト型水素化物は、これまで回転する容器内にて衝突を繰り返すステンレス製ボールの間で、ナノスケールに微細化・混合された出発原料を水素ガスと反応させる、メカノケミカル法で合成されていました。この合成法に対しては、出発原料の水素化反応過程やペロブスカイト型水素化物の形成過程を観測することは困難であり、形成機構は未解明のままでした。本実験では高輝度放射光X線回折測定により、出発原料と水素との直接反応によるペロブスカイト型水素化物の形成過程を観測することに成功しました。
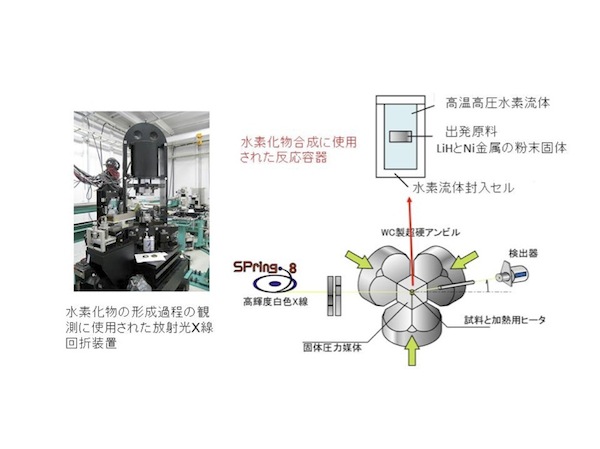
ペロブスカイト型水素化物LiNiH3はLiHとNiの粉体固体を水素化することによって合成されます。本研究ではペロブスカイト型水素化物の形成が、ステップ(Ⅰ)Niの水素化による水素化物NiHの形成、ステップ(Ⅱ)LiHとNiHの固溶体LiyNi1-yHの形成、ステップ(Ⅲ)固溶体の水素吸収によるペロブスカイト型水素化物LiNiH3の形成、の3段階で進むことが観測されました。
Fig.1はペロブスカイト型水素化物の形成が完了するまでのX線回折プロファイルの時間変化を示したものです。赤、緑、青で描いた回折プロファイルは上記ステップ(Ⅰ)、(Ⅱ)、(Ⅲ)の代表的なプロファイルです。
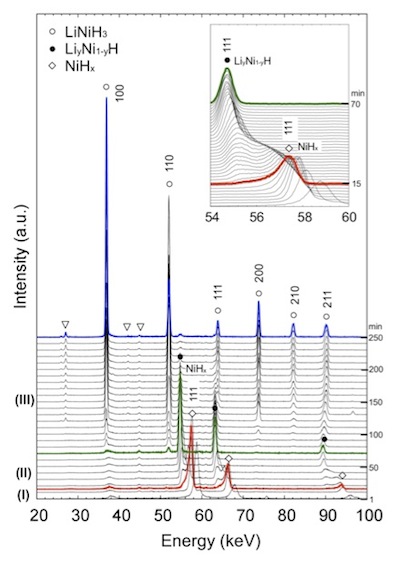
Fig.1
さらに、赤、緑、青の回折プロファイルの最強ピークの高さの時間変化をプロットしたものがFig.2で、時間とともにステップ(Ⅰ)→(Ⅱ)→(Ⅲ)と反応が進行することが解ります。
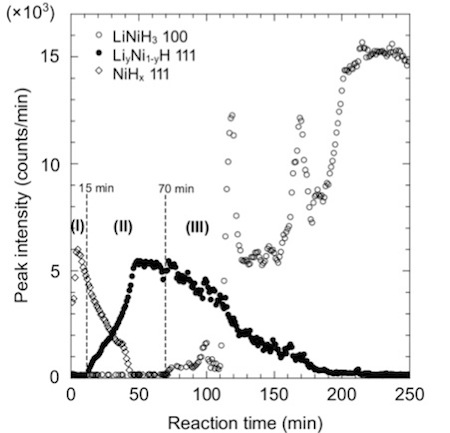
Fig.2
以上の高輝度放射光X線回折プロファイルの解析から、ペロブスカイト型水素化物の形成過程を結晶構造で示したのがFig.3です。
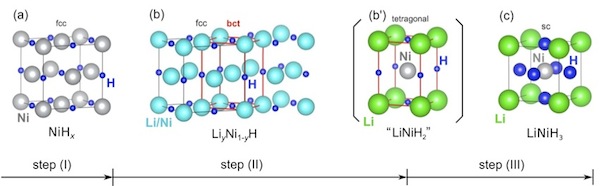
Fig.3
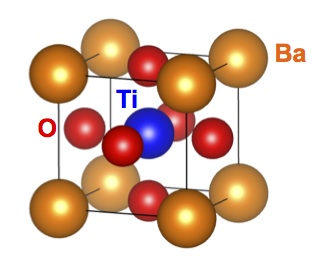
ステップ(Ⅱ)で形成される固溶体LiyNi1-yH(b)では金属格子点においてLi原子とNi原子が同じ割合で存在します。ステップ(Ⅲ)で形成されるLiNIH3(c)では立方体の中心に位置するNi原子が立方体の頂点に位置する8個のLi原子と、上下と側面の正方形の中心に位置する6個のH原子で囲まれています。両者の結晶構造から固溶体(b)からペロブスカイト型水素化物(c)への変化は中間体(b’)を経て進むものと推測されます。
解明された形成過程から、固溶体水素化物を形成しうる金属元素の組み合わせを選ぶことがペロブスカイト型水素化物の合成に繋がるとの設計・開発指針が得られました。この指針に基づいて新しいペロブスカイト型水素化物の合成研究を進めていきます。また、本合成法によって、従来のメカノケミカル法と比べて結晶性が良く、純度の高いペロブスカイト型水素化物が合成されることも解りました。新規合成されたペロブスカイト型水素化物の水素貯蔵や超伝導などの物性・機能性の評価研究を広範に進めます。
Ryutaro Sato, Hiroyuki Saitoh, Naruki Endo, Shigeyuki Takagi, Motoaki Matsuo, Katsutoshi Aoki, and Shin-ichi Orimo, "Formation process of perovskite-type hydride LiNiH3: In situ synchrotron radiation X-ray diffraction study" Applied Physics Letters (2013), Abstract
研究内容について
折茂慎一(おりも しんいち)
東北大学 原子分子材料科学高等研究機構・金属材料研究所
主任研究者・教授
| TEL : | 022-215-2093 |
|---|---|
| FAX : | 022-215-2091 |
齋藤寛之(さいとう ひろゆき)
独立行政法人日本原子力研究開発機構 量子ビーム応用研究部門
副主任研究員
| TEL : | 0791-58-2632 |
|---|---|
| FAX : | 0791-58-0311 |
報道担当
東北大学 金属材料研究所
事務部総務課庶務係
| TEL : | 022-215-2181 |
|---|---|
| FAX : | 022-215-2184 |
独立行政法人日本原子力研究開発機構
広報部報道課
| TEL : | 03-3592-2346 |
|---|---|
| FAX : | 03-5157-1950 |