

2014年03月31日
© 2013 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim
培養細胞は、その増殖を誘導する適切な足場があれば、機能性3次元組織を形成することができる。特に、ほとんど水でできている生体適合性ハイドロゲルは、ある種の細胞にとって有用な足場となるため、さまざまな用途への応用が期待されている。応用のためにハイドロゲルを硬化させるには、その水分含有量を減らすのが一般的だが、この方法では細胞の増殖を妨げてしまう可能性がある。さらに、ハイドロゲルは通常、電気を通さないため、増殖に電気刺激を必要とする細胞の培養には適さないという問題もある。
東北大学原子分子材料科学高等研究機構(AIMR)のSamad Ahadian助手らは、このたび、カーボンナノチューブを用いて丈夫で電気もよく通すハイドロゲルを作製した1。研究者らによると、このようなナノチューブの添加は、ハイドロゲルの機械的特性と電気的特性の両方を調節する方法のひとつであるという。
研究チームは、ベースとなるゼラチンメタクリレート(GelMA)ハイドロゲルに、多層カーボンナノチューブ(炭素原子でできた直径40~90ナノメートルの細い筒)を加えることによって、ハイドロゲルの剛性を2倍にした。
最初、ナノチューブはゲル中でランダムな方向を向いていたが、電場をかけることによって、これらを整列させることができた。次に、強い紫外光を照射して、GelMA分子間に結合を形成させて、ナノチューブをその場に固定した。ゲル中のナノチューブが整列してネットワークを形成することにより、ナノチューブの濃度に応じて、これらが整列していない場合の100~1000倍の電流をゲル中に流すことができた。
続いて、C2C12マウス筋芽細胞培養の足場として、このハイドロゲルを用いた。筋芽細胞は筋細胞の一種であり、融合して筋管を形成する。筋管が成熟すると細胞骨格が発達し、正常な筋組織のように振る舞うようになる。
ナノチューブ含有ゲル中に播種した筋芽細胞のうち、95パーセント以上が生存した。また、培養3日目には、細胞増殖が加速していることが確認された。これは、ナノチューブの添加により固定部位が増えたためであると考えられる。
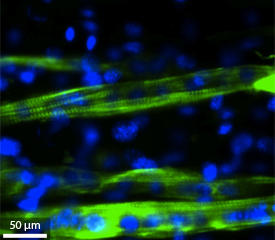
研究チームは、ハイドロゲル中に溝を刻むことにより、筋芽細胞が端と端を接して整列しやすくなるようにし、正常に収縮できる筋管の形成を促した。培養8日目には、溝に沿って筋細胞分化を促す低電圧をかけたが、最も顕著な効果が現れたのは、ナノチューブを整列させたハイドロゲルであった(図参照)。
ハイドロゲルで増殖させた筋組織は、多くの医学的応用が考えられる。「組織工学で作製した筋組織は、糖尿病治療薬候補を研究する効率的なプラットフォームとして利用することができます」とAhadian助手は説明する。「こうした組織は患者自身の筋細胞を使って作ることができるので、オーダーメイド医療への大きな一歩になるかもしれません。また、薬剤スクリーニングのために費用と時間のかかる動物実験を行う必要が無くなるかもしれません」。
Ramón-Azcón, J., Ahadian, S., Estili, M., Liang, X., Ostrovidov, S., Kaji, H., Shiku, H., Ramalingam, M., Nakajima, K., Sakka, Y. et al. Dielectrophoretically aligned carbon nanotubes to control electrical and mechanical properties of hydrogels to fabricate contractile muscle myofibers. Advanced Materials 25, 4028–4034 (2013). | article
このリサーチハイライトは原著論文の著者の承認を得ており、記事中のすべての情報及びデータは同著者から提供されたものです。